Les navires sont souvent exposés à des environnements marins très difficiles. En raison de l'environnement dans lequel ils opèrent, la coque du navire est souvent vulnérable à la corrosion environnementale.
La corrosivité de l'eau de mer en ce qui concerne la corrosion générale sur l'acier augmente avec l'augmentation de la température, la teneur en oxygène, la vitesse de l'eau, la teneur en contaminants corrosifs, les particules érodées et la conductivité. L'eau de mer contenant du sel forme un électrolyte parfait avec la coque du navire, entièrement constituée de fer (acier doux), pour former une cellule galvanique.

Qu'est-ce qu'une cellule galvanique et pourquoi la coque du navire se corrode-t-elle?
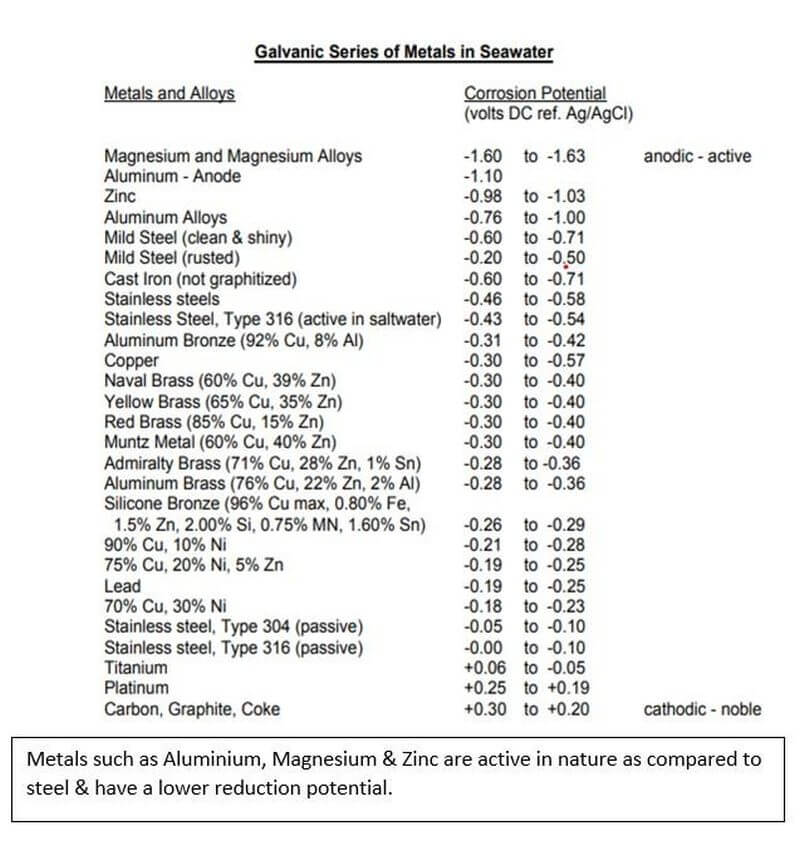
Lorsque 2 métaux différents sont en contact l'un avec l'autre en présence d'un milieu corrosif (électrolyte), le métal le plus actif de la série galvanique agit comme une anode et subit la corrosion. Cela signifie que, dans une série galvanique de métaux, le métal le plus actif agit comme anode et subit la corrosion et le métal le moins actif agit comme cathode et reste protégé.
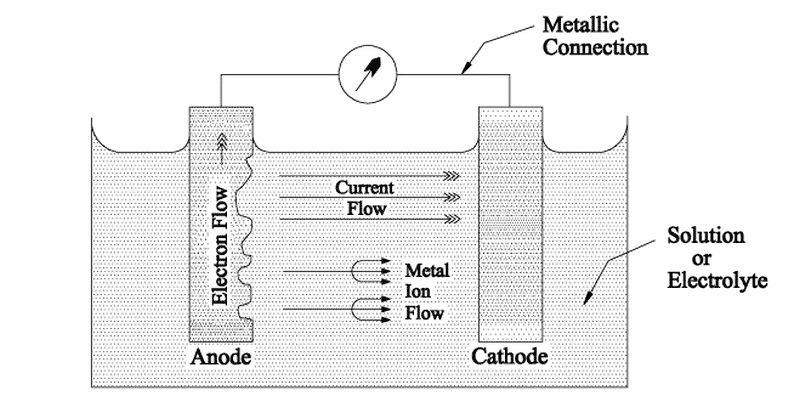
Si ces deux métaux sont placés dans l'eau de mer et sont en contact électrique direct, un courant traversera l'électrolyte du métal le plus actif (anode) au métal le moins actif (cathode). Ce courant électrique est appelé Courant de corrosion et n'est rien d'autre qu'un processus de transfert d'ions métalliques et d'électrons à partir de l'anode, qui se dissout et passe dans la solution. Cette cellule simple où se déroule le processus de corrosion est appelée cellule galvanique.
Alors, comment la corrosion se produit-elle sur les navires?
Les navires sont en acier; dont le composant principal est le fer. Le fer est un élément électrochimiquement positif et a tendance à abandonner les électrons pour devenir des ions libres.
1) La réaction anodique qui a lieu est 2Fe → 2Fe ++ + 4e-
2) L'eau de mer est composée d'oxygène et d'hydrogène et produit des ions hydroxyle électrochimiquement négatifs H2 O + O2 + 4 e- → 4 (OH) – qui peut accepter les électrons fournis par le fer.
3) Les ions fer se combinent avec les ions hydroxyle dans l'eau de mer pour former l'hydroxyde ferreux. 2 Fe ++ +2 (OH) – → 2 Fe (OH) 2. C'est ce qu'on appelle l'oxydation du fer.
4) Cet hydroxyde ferreux en présence d'un excès d'oxygène dans l'eau est oxydé pour former de l'oxyde ferrique et de l'eau, que nous appelons la rouille. 2 Fe (OH) 2 + O2 → Fe2 O3 + 2 H 2 O (rouille)
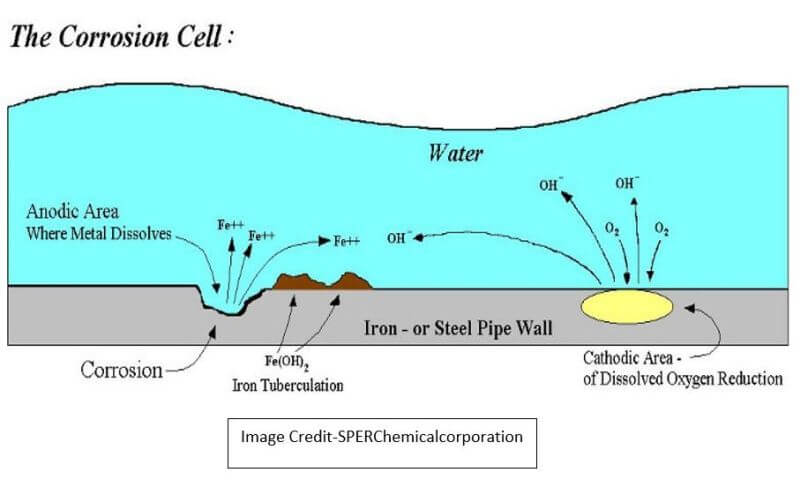
L'hétérogénéité de l'acier doux dans la coque du navire, ainsi que des facteurs tels que la non-uniformité de la plaque de coque, l'épaisseur, l'épaisseur et la qualité de la peinture, les variations des joints de soudure de la structure du navire, les métaux différents et la teneur en oxygène dans l'eau de mer se combinent pour causer zones dans la coque pour travailler les cathodes et les anodes et ainsi former une cellule galvanique.
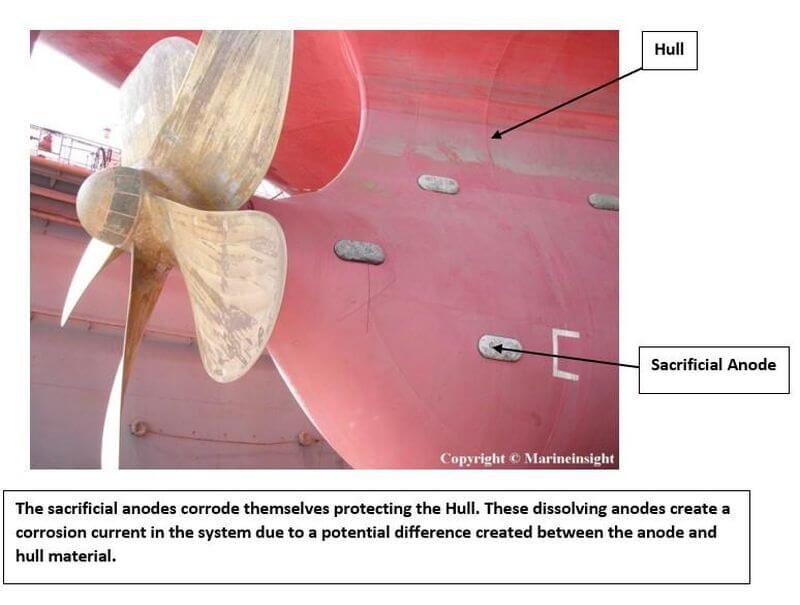
Avec la série galvanique, nous savons maintenant qu'un métal plus actif (anode) peut se corroder à la place du métal moins actif (cathode). En couplant la structure du navire avec un métal plus actif tel que le zinc ou le magnésium, une cellule galvanique est créée dans laquelle le métal actif fonctionnant comme une anode fournit un flux d'électrons à la structure qui devient alors la cathode. La cathode est protégée et l'anode se dissout progressivement, ce qui est appelé anode sacrificielle.
Des éléments tels que le zinc, l'aluminium, le magnésium ou leurs alliages sont utilisés comme anode sacrificielle pour protéger l'élément parent comme le fer ou l'acier qui forme la cathode. Cependant, ces anodes sacrificielles présentent certains inconvénients tels qu'une maintenance accrue due au remplacement tous les 5 ans, une résistance accrue à la coque et aucun moyen approprié pour détecter si les anodes fonctionnent correctement.
Le besoin du CIPC
Nous savons maintenant de la cellule galvanique et des anodes sacrificielles, qu'une différence de potentiel entre 2 électrodes est nécessaire pour que les courants de corrosion se produisent. Ces courants de corrosion dissolvent l'anode dans l'électrolyte.
Mais en l’absence de différence de potentiel à l’intérieur de la coque du navire, le courant de corrosion sera au minimum et il n’y aura pas de corrosion.
C'EST CE QUE FAIT L'ICCP. IL FAIT LA COQUE POUR RESTER TOUJOURS CATHODE en maintenant la différence de potentiel au minimum et en introduisant un courant opposé au courant de corrosion naturel, protégeant ainsi l'anode et évitant la corrosion.
Protection cathodique actuelle impressionnante
Les systèmes de protection cathodique à courant imposé sont la solution technologiquement avancée et à long terme aux problèmes de corrosion et sont considérés comme une alternative supérieure aux systèmes d'anode sacrificielle.
Dans l'ICCP, le métal à protéger est connecté à une anode insoluble et le courant passe à l'aide d'une source DC opposée au courant de corrosion, de sorte que le métal corrodant se
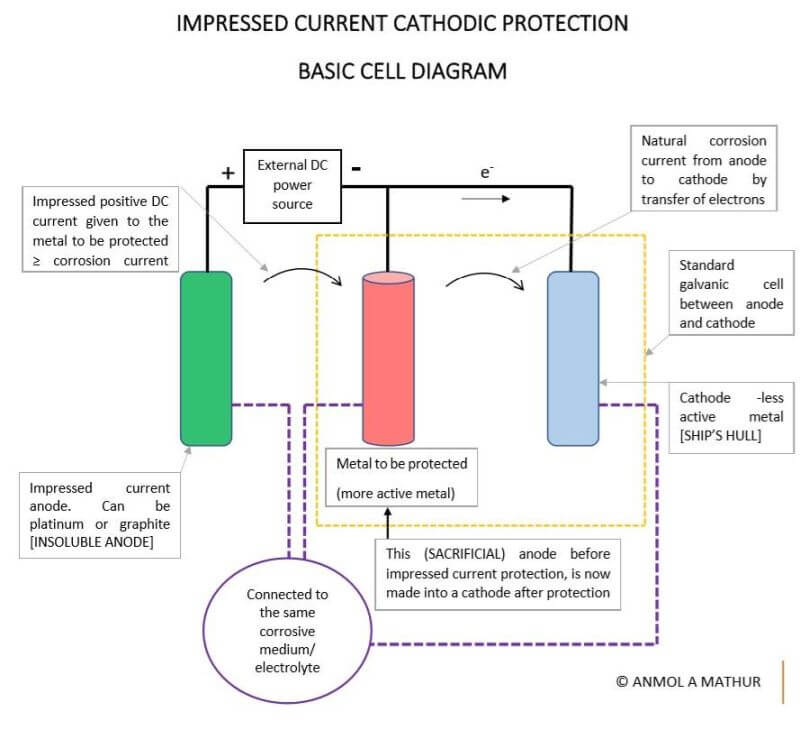
converti d'anode en cathode et protégé contre la corrosion. Cette anode insoluble peut être du platine, du titane platiné ou tout autre élément inerte.
Le diagramme ci-dessus est une cellule galvanique similaire d'une anode (métal plus actif) et d'une cathode (métal moins actif) avec quelques modifications. Ici, une anode à courant imposé insoluble est ajoutée dans le système. Dans des circonstances normales, sans l'anode insoluble, un courant de corrosion est établi qui corrode l'anode, cependant, dans ce cas, nous passons un courant continu opposé au courant de corrosion naturel entre l'anode et la cathode.
Ce courant continu doit être égal ou légèrement supérieur au courant de corrosion naturel pour que l'anode soit maintenant protégée et ne se corrode pas.
Le même principe est appliqué aux navires.
Ici, un point de contact est pris sur la coque du navire et est connecté à une électrode de référence. Cette électrode de référence est un métal insoluble complètement passif. L'électrode de référence mesure le courant de corrosion naturel qui n'est rien d'autre que la différence de potentiel entre la coque et cette cellule de référence.
Nous devons mesurer ce courant de corrosion dans la coque, afin de fournir un courant continu qui est soit égal ou légèrement supérieur à celui-ci (dans le sens opposé) à l'anode à courant imposé.
Ceci, à son tour, fournit un COURANT DE PROTECTION à la coque du navire, faisant de la coque une cathode protégée contre la corrosion.
L'opération ICCP et ses composants
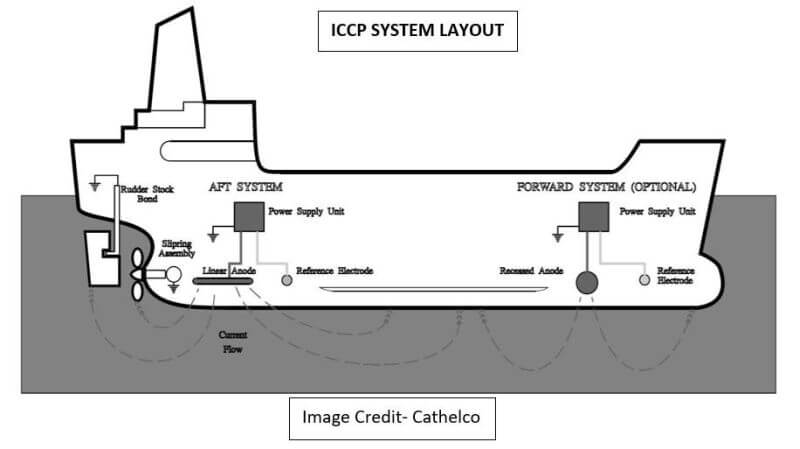
1) Unité d'alimentation de sortie DC 24 V et panneau de commande
L'alimentation CC peut comprendre un redresseur convertissant une alimentation CA de 440 V en courant CC.
Les plus grands navires ont généralement 2 unités d'alimentation électrique à l'avant et à l'arrière. L'unité d'alimentation est également connue sous le nom de panneau Quantum ICCP et contient un réseau de thyristors et de PCB qui surveillent les paramètres de tension et de courant des cellules de référence et envoient en conséquence des signaux aux anodes de courant imposées. Ces unités d'alimentation ont une configuration maître-esclave entre les unités avant et arrière et les performances peuvent être surveillées à partir du panneau de contrôle ECR. Le panneau de commande est incorporé avec des alarmes pour des lectures anormales.

2) Anodes à courant imposé
Les anodes à courant imposé sont généralement constituées de matériaux insolubles solides comme le titane. Ils peuvent être en forme de disque ou en forme de bande. Soit 2 ou 4 unités sont placées symétriquement vers l'avant et l'arrière du navire.
Les anodes sont soudées sur des plaques doubleuses sur la surface de la coque de manière à affleurer complètement la plaque extérieure de la coque. Ce matériau d'anode ne sert que de source d'électrons à la coque et n'est pas consommé pour fournir ce courant de protection.
3) Cellule de référence en zinc
Le potentiel électrique est surveillé par un ensemble d'électrodes de référence qui est installé à bâbord et à tribord entre les anodes où le potentiel le plus bas possible est susceptible de se produire afin de détecter le moindre des courants de corrosion entre la coque et l'eau de mer. Cette lecture est renvoyée au panneau de commande qui ajuste automatiquement la sortie de l'anode de courant imprimé.
Ils sont reliés par des cosses de câble et des joints et sont boulonnés à travers un corps de batardeau sur la surface de la coque. Ces cellules de référence en zinc sont de nature très stable et donnent une référence stable dans laquelle les potentiels de coque et de mer peuvent être mesurés avec de petits flux de courant dans le système. Ces électrodes sont totalement interchangeables.
La vidéo ci-dessus donne une image plus claire du travail de l'ICCP à bord.
4) Panneau de surveillance à distance
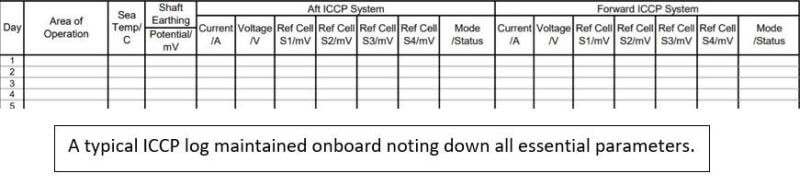
Un panneau de surveillance à distance dans la salle de commande du moteur est fourni où les paramètres ICCP sont surveillés et enregistrés quotidiennement. Il faut s'assurer que la source d'alimentation ICCP est éteinte lorsque le navire accoste. Ou bien il y a une chance que les courants du système ICCP du navire et du rivage interagissent les uns avec les autres, causant des dommages à la peinture de la coque. Un excès de courant imprimé à la surface de la coque peut entraîner un décollement de la peinture.
5) Câble de liaison de gouvernail
Pour permettre au gouvernail de recevoir une protection contre la corrosion par le biais de l'ICCP, un câble de liaison en caoutchouc flexible est utilisé avec une extrémité attachée au sommet de la mèche de gouvernail et l'autre extrémité à la structure de la coque à l'aide de cosses de câble ou de plaques à oeil. Cela forme une liaison électrique dédiée.
6) Ensemble de mise à la terre de l'arbre d'hélice avec voltmètre mv de coque d'arbre
Même sur les navires équipés du ICCP, les roulements d'arbre d'hélice sont vulnérables à la corrosion due à l'érosion par étincelles. En effet, l'arbre d'hélice rotatif est isolé électriquement de la coque par le film d'huile de lubrification dans les roulements et l'utilisation de roulements non métalliques dans l'arbre de queue. En raison de cette isolation créée, un potentiel électrique se développe entre l'arbre et la coque, ce qui peut faire circuler de forts courants dans le roulement.
De forts courants peuvent également circuler dans les paliers principaux et le palier de butée et provoquer des marques de piqûres entraînant des dommages au moteur principal.

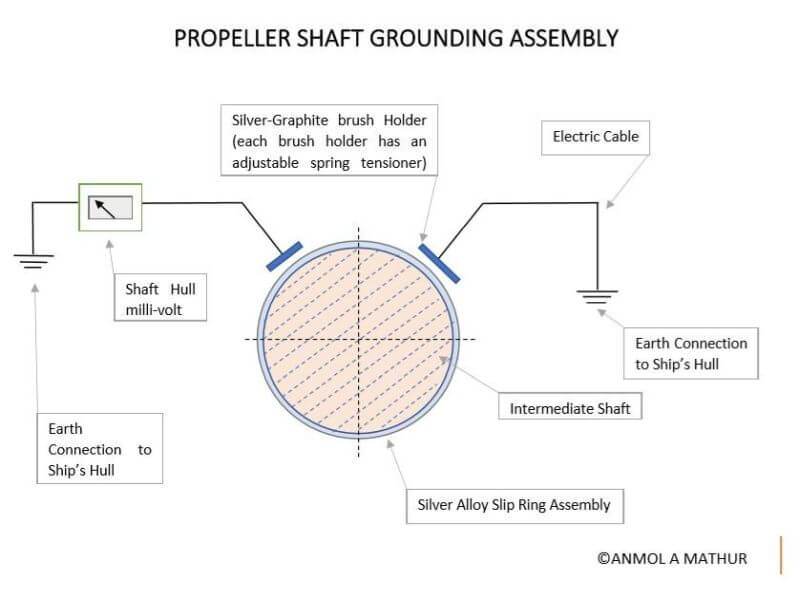
Ce problème est éliminé en mettant à la terre l'arbre d'hélice sur la coque à l'aide d'une bague collectrice et d'une brosse de contact.
L'ensemble de mise à la terre de l'arbre se compose d'une paire de brosses composites à haute teneur en argent / graphite montées dans un porte-balais, fonctionnant sur une bague en cuivre avec une piste d'incrustation en bande métallique en alliage d'argent massif.
L'ensemble de mise à la terre en alliage d'argent offre une excellente continuité électrique.

La bague collectrice d'arbre en alliage d'argent est fournie sous la forme d'un ensemble de 2 moitiés avec un dispositif de serrage afin de faciliter l'installation.
Un millivoltmètre compact est installé pour surveiller le potentiel entre le puits et la coque et vérifier l'efficacité du système. Le compteur est situé dans une position pratique pour la surveillance par l'équipage.

Une lecture inférieure à 50 mV est considérée comme favorable.
Passage d'eau douce
Lorsqu'un navire passe de l'eau de mer à l'eau douce, sa conductivité électrique diminue et sa résistivité augmente. En raison de la conductivité réduite, la cellule de référence ne sera pas en mesure de détecter une différence de potentiel. À ce stade, il est important de limiter le courant de protection de sortie des anodes à courant imposé.
Pendant le passage en eau douce, la commande automatique dans le bloc d'alimentation de l'ICCP augmentera sa tension redressée au maximum afin de limiter le courant imposé et d'éviter une surprotection et de sauver la coque.
Aux terminaux, le ICCP du navire, s'il est allumé, tentera de protéger la jetée et augmentera ainsi le courant dans le système, ce qui peut entraîner une surcharge. Par conséquent, la source d'alimentation ICCP est toujours éteinte dans le port.
J'espère que cela clarifie la plupart des doutes sur le système cathodique à courant imposé. Le ICCP étant des machines très sous-estimées est souvent négligé dans la salle des machines et est révisé et inspecté généralement en cale sèche.
Cependant, cela est préféré par la plupart des armateurs car il contribue à réduire la consommation de carburant, à augmenter la vitesse du navire en raison de la résistance réduite de la coque et à maintenir la qualité de la coque en métal pendant des intervalles de temps plus longs, augmentant ainsi les intervalles de maintenance et la rentabilité.
Vous avez des doutes?
N'hésitez pas à demander dans le commentaire ci-dessous